生物医学工程
-
梁文轩
特任研究员、博士生导师
梁文轩,特任研究员,博士生导师,入选中科院人才计划。本硕毕业于清华大学生物医学工程系,博士毕业于约翰斯霍普金斯大学(Johns Hopkins University)生物医学工程系,在美国哥伦比亚大学祖克曼研究所(Zuckerman Institute)完成博士后训练。
电子邮箱:liangwenxuan(AT)ustc.edu.cn
联系地址:江苏省苏州市工业园区仁爱路188号
课题组主页:https://faculty.ustc.edu.cn/liangwenxuan/
课题组简介:本课题组专注于生命科学(尤其是神经科学/脑科学)和临床诊疗中的活体光学显微方法、仪器与应用研究,属于典型的理-工-生-医交叉学科。
代表性研究方向:具体(代表性)研究项目和应用方向包括但不限于:
1. 面向跨尺度生理动态观测的大视场共焦斜光片扫描(SCAPE)显微成像方法
2. 自由行为小动物(如斑马鱼)全脑神经活动实时观测与光遗传学操控方法、平台与算法
3. 面向实时原位病理学成像的 手持式三维显微成像探头(无创/微创)
4. 面向消化道等场景的荧光内窥显微技术与仪器研究
招生信息
推免/统考(硕士或博士)研究生
入学渠道(录取专业):
苏州高等研究院 生物医学工程学院(生物医学工程 / 电子信息)
科大本部物理学院(应用物理学 / 电子信息)
本科生(大研 / 毕设)
课题组提供科研训练与竞赛支持,欢迎来自以下专业的本科生:
物理 / 光学工程
光电信息 / 精密仪器 / 电子信息 / 自动化 / 机械
计算机 / AI
生物医学工程 等
可参与方向包括(但不限于):显微成像系统设计与搭建,三维图像时空联合分析与处理算法,神经成像实验等。
如对本课题组感兴趣或有任何问题,欢迎邮件或 QQ(寺泠迩柳绮驷珥旗榴)联系。
给未来同学的一些问题与回答(FAQ)
1. 课题组主要在做什么?可以简单解释吗?
简单来说,我们在做两件事:(1)发明显微镜(新的成像技术);(2)用这些显微镜研究神经系统或临床疾病。例如:看清活体小动物大脑里成千上万个神经元同时活动,或开发可以在人体内使用的显微成像设备。
2. 什么是光学显微成像 / 共焦斜光片扫描(SCAPE)?难吗?
可以简单理解为:一种“可以在三维空间里高速拍摄活体”的显微技术。相比传统显微镜,不用移动物镜或者样品,即可逐层扫描,三维速率大幅提升,可以实时看到动态过程(比如血流、神经活动)。刚开始不需要完全理解,我们(导师+学长学姐等)会从基础慢慢带。
3. 我在课题组会做什么?
根据你的兴趣,可能会参与:搭建或改进显微成像系统,写程序处理三维图像数据,做仿真优化光学设计,或参与生物实验(如斑马鱼)——总之,一般是“实验 + 算法”结合。
4. 我需要很强的基础吗?不同专业可以吗?
完全可以跨专业。常见背景包括:生物医学工程 / 物理 / 光学 / 光电信息 / 电子信息 / 精密仪器 / 机械 / 自动化 / 计算机 等。
我们更看重:严谨为学,诚信为人,主动性,学习能力,团队协作精神。
5. 更偏学术还是工业发展?
两条路径都适合,也都支持:
学术:读博、科研机构、出国深造
工业:科研仪器、半导体、医疗器械、生物科技公司等
本方向在产业界需求也很强(具体见下方lab alumni列表)
6. 有没有机会参与创新创业?
有。课题组研究方式本身就具备产业转化潜力(科研仪器、医疗设备等)。也鼓励同学参与创新创业项目,产学研合作等。
组内多名研究生在科大“庆峰杯”、安徽省“挑战杯”、苏州独墅湖科教创新区“慧湖青创计划”等创新创业赛事取得佳绩,以及获批多项科大雏鹰基金、苏高院学生创新创业项目等。
Alumni(毕业生去向)
课题组往届研究生(从2022级开始招生)毕业 / 准毕业去向:
· Shen, B. (2022级硕士) → 常州纵慧芯光半导体科技有限公司,光机工程师
· Cao, Z. (2022级硕士) → 组内转博
· Huang, Y. (2022级硕士) → 组内转博
· Zhu, J. (2023级硕士) → 聚光科技(杭州)股份有限公司,研究工程师
· Zhang, C. (2023级硕士) → 国仪量子技术(合肥),系统工程师(电镜)
以往研究成果(已发表)
1. 设计构建了国际首例面向临床原位在体实时三维病理学显微的小型化SCAPE显微镜,在主物镜孔径光阑直径减小2/3、整机占地面积缩小4/5的同时,仍取得了与台式SCAPE设备同等水平的荧光收集效率和三维分辨率(0.81 µm × 1.07 µm × 2.10 µm),实现了仅靠内源性自体荧光的在体大范围全景体积成像。
动物实验表明,该小型SCAPE显微镜能够仅靠自体荧光清晰可视化肝、肾等小鼠器官组织的细胞级微观结构(如下图c所示);在健康志愿者无标记的舌头上仅需6.4毫瓦激发功率便能取得4.8体积/秒的三维体积率,且在志愿者自由伸缩舌头时,能够从所得的高速“三维体数据流”中直观而准确地估计出相邻体数据块之间的三维位移,进而经配准融合生成覆盖若干毫米范围的三维全景拼接图像(下图d)——由此验证了该小型SCAPE显微镜对活体组织运动出色的抗干扰能力和临床应用潜力。
延伸阅读:“无需切片、胜似切片”:中国学者开发小型化在体实时三维显微成像设备

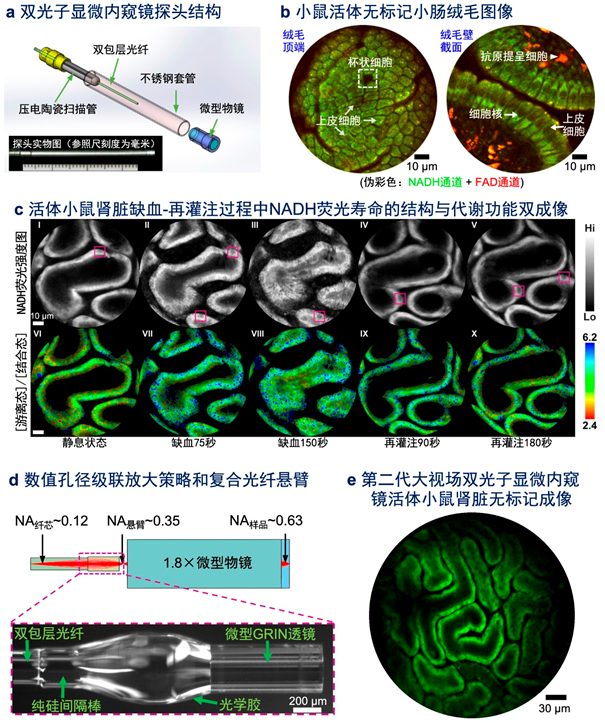
2. 主导研发了两代基于柔性光纤扫描的微型双光子显微内窥成像技术:
2.1. 系统深入地研究了制约双光子显微内窥镜成像信噪比的关键因素,并研究提出了相应的解决方案,构建了直径仅2.2毫米的“第一代”微型双光子显微内窥探头(见下图a),将探测灵敏度相对于此前设计提升了20倍以上,突破了长期制约光纤双光子内窥技术的成像信噪比瓶颈,实现了可实用的活体无标记实时双光子内窥显微成像(见下图b)。
2.2. 提出了数值孔径级联放大的设计策略,显著提升了第二代光纤扫描双光子显微内窥镜的空间-带宽-成像速度三重积。
2.3. 发展了能同步采集光学氧化还原比和NADH荧光寿命的无标记双光子显微内窥代谢成像方法,能够跟踪活体小鼠皮质肾小管上皮细胞在缺血-再灌注过程中氧化还原比的动态变化和胞内游离态NADH与结合态NADH的丰度涨落(如下图c所示),首次展示了在活体动物模型上的内窥式双光子无标记结构与代谢功能双成像。
近五年主要学术论文:
1. Zixian Cao, Jiapeng Zhu, Cheng Zhang, Qianqian Wang, Yankan Huang, Wei Liu, Bingxin Shen, Yuming Chai, Zhaomin Zhong, Li He, Quan Wen, Han Wang, and Wenxuan Liang#. Mesoscopic SCAPE Microscope with a Rescanned, Super-oblique Illumination Plane. bioRxiv 2025.04.25.650616; https://doi.org/10.1101/2025.04.25.650616
2. Shen B, Cao Z, Huang Y, Zhu J, Huang H, and Liang W#. Computationally designing a dual-aspheric compound lens towards multi-depth endomicroscopy imaging. Applied Physics Letters 126 (22), 223701 (2025) #Correspondence https://doi.org/10.1063/5.0268424
3. Liang W#, Liu Y, Guan H, Sakulsaengprapha V, Luby-Phelps K, Mahendroo M, and Li X. Cervical Collagen Network Porosity Assessed by SHG Endomicroscopy Distinguishes Preterm and Normal Pregnancy - a Pilot Study. IEEE Transactions on Biomedical Engineering 72(2), 777-785 (2025) #Correspondence https://doi.org/10.1109/TBME.2024.3472015
4. Li K, Yang J, Liang W, Li X, Zhang C, Chen L, Wu C, Zhang X, Xu Z, Wang Y, Meng L, Zhang Y, Chen Y, Zhou SK. O-PRESS: Boosting OCT axial resolution with Prior guidance, Recurrence, and Equivariant Self-Supervision. Medical Image Analysis, 99, 103319 (2025) https://doi.org/10.1016/j.media.2024.103319
5. Hall G*, Liang W*‚#, Bhujwalla ZM, and Li X#. SHG fiberscopy assessment of collagen morphology and its potential for breast cancer optical histology. IEEE Transactions on Biomedical Engineering 71(8), 2414-2420 (2024). *Equal contribution, #Correspondence https://doi.org/10.1109/TBME.2024.3372629
6. Liang W, Chen D, Guan H, Park HC, Li K, Li A, Li MJ and Li X. Label-Free metabolic imaging in vivo by two-photon fluorescence lifetime endomicroscopy. ACS Photonics, 9(12), 4017-4029 (2022) https://doi.org/10.1021/acsphotonics.2c01493
7. Patel KB, Liang W, Casper MJ, Voleti V, Zhao HT, Perez-Campos C, Liu JM, Coley SM, and Hillman EMC. High-speed light-sheet microscopy for the in-situ acquisition of volumetric histological images of living tissue. Nature Biomedical Engineering 6, 569-583 (2022) https://doi.org/10.1038/s41551-022-00849-7
8. Liang W, Park HC, Li K, Li A, Chen D, Guan H, Yue Y, Gau YT, Bergles DE, Li MJ, Lu H, and Li X. Throughput-speed product augmentation for scanning fiber-optic two-photon endomicroscopy. IEEE Transactions on Medical Imaging 39(12), 3779-3787 (2020) https://doi.org/10.1109/TMI.2020.3005067
9. Li K*, Liang W*, Yang Z, Liang Y, and Wan S. Robust, accurate depth-resolved attenuation characterization in optical coherence tomography. Biomedical Optics Express 11(2), 672-687 (2020) *Equal contribution https://doi.org/10.1364/BOE.382493
